メディカルバイオサイエンス学科
 伊藤 正惠(いとう・まさえ)
伊藤 正惠(いとう・まさえ)
Masae Itoh
専門分野/微生物学(ウイルス学)研究キーワード/ウイルス、感染、増殖、病原性、宿主指向性、遺伝子組み換え、ウイルス工学
職位:学長、教授
学位:医学博士(神戸大学)
- 神戸大学大学院医学研究科博士課程修了
- マールブルグ・フィリップス大学ウイルス研究所研究員、神戸大学医学部講師、大阪府立公衆衛生研究所主任研究員を歴任
研究テーマ
2019年12月に中華人民共和国武漢市で確認された新型コロナウイルス(SARS-CoV-2)は、世界中に拡散し、1億人以上が感染、200万人以上が死亡する世界的大流行(パンデミック)を引き起こしている(2021年3月現在)。これまでも、ウイルスによる感染症は大きな問題となってきた。2009年から2010年にかけて、新型インフルエンザウイルスがパンデミックを引き起こし、2014年西アフリカで発生したエボラウイルス病は、致死率が高く危機的な大流行となった。新型コロナウイルスの感染が続く中、日本各地では高病原性鳥インフルエンザウイルスのニワトリへの感染も頻発している。AIDS(後天性免疫不全症候群)、麻疹、C 型肝炎や家畜の口蹄疫も原因はウイルスである。ウイルスは宿主となるヒトなどの細胞に侵入し、その機能を借りて自己を増殖させる。新型コロナウイルスでは、ようやくワクチン接種が開始され、感染の収束が期待されているが、診断法やワクチン、抗ウイルス剤を開発し、ウイルス感染症を克服するためには、ウイルスの増殖機構を分子レベルで解明し理解することが不可欠である。
<麻疹ウイルス増殖機構の解析>
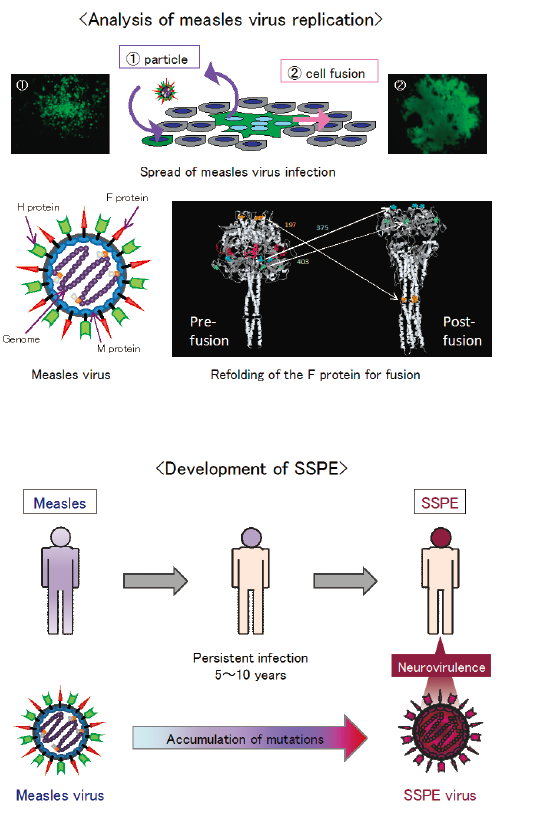 麻疹ウイルスの感染は、①粒子を形成して未感染細胞に吸着侵入する、②感染細胞が隣接する細胞と直接融合する、の2経路で拡大する。麻疹ウイルスがどちらの経路を優先するかは、ウイルスM蛋白が関わる子孫粒子の出芽能力とウイルスF蛋白により引き起こされる細胞膜融合能力の強さに左右されるが、その詳細な分子メカニズムは明らかではない。さらにこれらの過程には、レセプター結合能を持つウイルスH蛋白が必須である。粒子形成能と細胞融合能が様々に異なる変異株を比較するという手法で、これらのウイルス蛋白間、あるいは宿主細胞因子との相互作用を中心に解析を進めている。
麻疹ウイルスの感染は、①粒子を形成して未感染細胞に吸着侵入する、②感染細胞が隣接する細胞と直接融合する、の2経路で拡大する。麻疹ウイルスがどちらの経路を優先するかは、ウイルスM蛋白が関わる子孫粒子の出芽能力とウイルスF蛋白により引き起こされる細胞膜融合能力の強さに左右されるが、その詳細な分子メカニズムは明らかではない。さらにこれらの過程には、レセプター結合能を持つウイルスH蛋白が必須である。粒子形成能と細胞融合能が様々に異なる変異株を比較するという手法で、これらのウイルス蛋白間、あるいは宿主細胞因子との相互作用を中心に解析を進めている。
<亜急性硬化性全脳炎(SSPE)発症メカニズムの解明>
SSPEは、麻疹に罹患した人の数千人に1人が発症する致死性ウイルス感染症である。麻疹完治後5~10年の長い間、麻疹ウイルスが脳内の中枢神経系に持続感染し、変異の蓄積により神経病原性を獲得してSSPE ウイルスへと変貌する。SSPEウイルスはその特徴として、粒子形成能を欠失して細胞融合能を亢進させているが、持続感染の成立から病原性獲得へと至る分子メカニズムは、その変異の多さのため未だ明らかではない。麻疹罹患後5年という比較的短期間でSSPE を発症した患児から変異の少ないSSPE ウイルスを分離し、麻疹ウイルスからSSPE ウイルスへと至る変異過程の解明を目指している。
| 研究の応用領域 | 産官学連携で求めるパートナー |
|---|---|
| 抗ウイルス剤、ウイルス診断法の開発 | 抗ウイルス剤、ウイルス診断法開発の関連企業、大学、国・地方自治体の研究機関 ウイルス感染症の基礎・応用・臨床研究者 |
Topics of research
Emergence of a pneumopathogenic coronavirus was reported from Wuhan China in December 2019. The virus named severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) quickly spread all over the world, which resulted in the declaration of pandemic by World Health Organization causing more than hundred million infected and more than 2 million deceased persons (as of March 2021). Emerging or re-emerging infectious diseases caused by viruses is one of the most anxious issues world-wide today. An influenza virus originated from swine H1N1 virus spread around the world shortly after the first invasion into human in April 2009, and in 2014 outbreak of Ebola virus disease in western district of Africa brought a critical pandemic with high mortality. At present under the prevalence of SARS-CoV-2 in human, infection of highly pathogenic avian influenza virus often occurs in chicken ranch in Japan. Causative agents of many serious diseases such as acquired immune deficiency syndrome( AIDS), measles, hepatitis C and cattle foot-and-mouth disease are also viruses. Viruses replicate and grow by introducing their genome into their host cells and then making use of the functions there such as RNA polymerases, ribosome, vesicular transport systems and so on. Therefore, to develop rapid diagnosis systems, effective vaccines and anti viral drugs to overcome viral diseases, it is required to understand the molecular mechanisms of the viral replication and to set the target on the biological processes specific for viral replication.
<Analysis of measles virus replication>
Measles viruses spread their infection by different 2 ways: firstly, they form progeny particles which adsorb and penetrate the uninfected cells apart from the infected cells, and secondly, they fuse the infected cells with the adjacent cells directly introducing viral genomes, mRNAs and proteins. Which way a measles virus adopts as a dominant route of infection depends on the abilities of the M protein to form particles as well as of the F protein to induce membrane fusion, but the precise mechanism is not yet elucidated. In our laboratory, comparing various measles virus strains with different particle-forming and fusion activities, analyses of the interaction especially between viral components and host cell factors are on the way.
<Pathogenicity of subacute sclerosing panencephalitis (SSPE) virus>
SSPE is a fatal sequela associated with measles. The risk of developing SSPE was reported as 1 case per 1,300 ~ 3,300 cases of acute measles after a long latency period of 5 to 10 years. SSPE is developed by persistent infection of the central nervous system with measles virus, during which the parental measles virus acquires neurovirulence by accumulation of mutations on the genome. SSPE viruses, without exception, have lost the ability to form virus particles and obtained strong cell-cell fusion activity, however, the mechanism how SSPE viruses establish the persistent infection followed by the acquirement of neural pathogenicity is still unraveled due to the numerous mutations on their genome. Isolating a SSPE strain with the limited number of mutations from a patient who developed SSPE 5 years after acute measles, an investigation to identify mutations intrinsically substantial for the development of SSPE has been undertaken in our laboratory.
主な業績論文等
- Kitagawa, Y., Sakai, M., Funayama, M., Itoh, M. and Gotoh, B. Human Metapneumovirus M2-2 Protein Acts as a Negative Regulator of Alpha Interferon Production by Plasmacytoid Dendritic Cells. J. Virol., 91(20): e00579-17. (2017)
- Satoh, Y., Yonemori, S., Hirose, M., Shogaki, H., Wakimoto, H., Kitagawa, Y., Gotoh, B., Shirai, T., Takahashi, KI. and Itoh, M. A residue located at the junction of the head and stalk regions of measles virus fusion protein regulates membrane fusion by controlling conformational stability. J. Gen. Virol., 98(2): 143-154. (2017)
- Satoh, Y., Hirose, M., Shogaki, H., Wakimoto, H., Kitagawa, Y., Gotoh, B., Takahashi, K. and Itoh, M. Intramolecular complementation of measles virus fusion protein stability confers cell-cell fusion activity at 37 °C. FEBS Lett., 589(1): 152-158. (2015)
- Yamaguchi, M., Kitagawa, Y., Zhou, M., Itoh, M. and Gotoh, B. An anti-interferon activity shared by paramyxovirus C proteins: inhibition of Toll-like receptor 7/9-dependent alpha interferon induction. FEBS Lett., 588(1): 28-34. (2014)
- Wakimoto, H., Shimodo, M., Satoh, Y., Kitagawa, Y., Takeuchi, K., Gotoh, B. and Itoh, M. F-Actin Modulates Measles Virus Cell-Cell Fusion and Assembly by Altering the Interaction between the Matrix Protein and the Cytoplasmic Tail of Hemagglutinin. J. Virol., 87(4): 1974-1984. (2013)






